Tumori, la scelta della cura parte dalla profilazione genomica. Ecco il nuovo modello dell’oncologia

Nel Vecchio Continente il 51% delle donne e il 39% degli uomini superano la malattia. Giordano Beretta, Presidente AIOM: “Queste terapie innovative colpiscono le alterazioni molecolari, indipendentemente dall’organo malato”. Servono team multidisciplinari per intrepretare i test

Milano, 26 dicembre 2020 – In Europa 25 milioni di persone vivono dopo la diagnosi di tumore (su una popolazione complessiva di circa 500 milioni di abitanti). E in un decennio, dal 1990 al 2000, la probabilità di guarire è aumentata del 10% per la maggior parte delle neoplasie, con incrementi significativi soprattutto per quelle della prostata (dal 22% nel 1990 al 63% nel 2000), della mammella (dal 50% al 66%), del colon-retto (dal 41% al 52% nelle donne e dal 37% al 49% negli uomini) e della tiroide (dal 76% all’87% nelle donne e dal 57% al 70% negli uomini).
Complessivamente la probabilità di guarire dopo un tumore, in Europa, è del 51% nelle donne e del 39% negli uomini. Risultati importanti, che si legano al nuovo paradigma della lotta ai tumori che si sta spostando dall’organo colpito dalla malattia all’alterazione molecolare, in grado di predire la sensibilità alle terapie mirate o all’immunoterapia. E i farmaci agnostici sono considerati “jolly”, proprio perché colpiscono in maniera selettiva alcune mutazioni genetiche, indipendentemente dall’organo interessato dalla patologia.
Per rendere effettivo il nuovo modello dell’oncologia di precisione devono essere resi operativi, su tutto il territorio, i Molecular Tumor Board (MTB), cioè i team multidisciplinari, indispensabili per interpretare i risultati dei test molecolari e scegliere la terapia migliore. Oggi sono attivi solo una decina di MTB. E deve essere istituita una Piattaforma Nazionale Genomica, per condividere i dati delle analisi molecolari e consentire a tutti i pazienti l’accesso alle terapie innovative. La richiesta viene dall’Associazione Italiana di Oncologia Medica (AIOM), oggi in una conferenza stampa virtuale, realizzata con il sostegno non condizionato di Bayer.
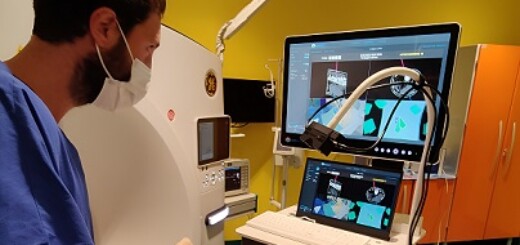
“L’oncologia è di fronte a profondi mutamenti, che stanno portando all’affermazione di un nuovo modello, definito mutazionale – spiega Giordano Beretta, Presidente Nazionale AIOM e Responsabile Oncologia Medica Humanitas Gavazzeni di Bergamo – Il punto chiave del nuovo processo è rappresentato dalla profilazione genomica e, quindi, dall’individuazione della mutazione ‘driver’ e del carico mutazionale, che guidano la scelta della terapia, indipendentemente dalla sede del tumore, dall’età e dal sesso del paziente. I farmaci agnostici sono correlati al modello mutazionale: non sono studiati e testati per la loro efficacia su uno specifico tipo di cancro, ma colpiscono selettivamente alcune mutazioni genetiche, che possono essere responsabili di diverse neoplasie, in diversi organi”.
In un’analisi su 500 pazienti con tumori di diverso tipo in stadio avanzato sottoposti a profilazione genomica dal MD Anderson Cancer Center (Houston, USA), nel 30% dei casi è stata riscontrata un’alterazione genetica che può essere bersaglio di trattamenti specifici (definita ‘actionable’). E in uno studio clinico prospettico su 843 persone con tumore avanzato, un’alterazione ‘actionable’ è stata identificata, grazie all’analisi genomica, nel 49% dei pazienti.
“La presenza di alterazioni molecolari ricorrenti nei tumori richiede la profilazione genomica con strumenti diagnostici che forniscano informazioni per tracciare il profilo molecolare delle varie forme tumorali, sia in termini quantitativi che qualitativi – afferma Antonio Russo, Membro Direttivo Nazionale AIOM e Ordinario di Oncologia Medica, DICHIRONS – Università degli Studi di Palermo – I pazienti candidati al trattamento con farmaci agnostici dovrebbero essere selezionati sulla base della presenza delle alterazioni molecolari, individuate attraverso test agnostici. In particolare, il test di sequenziamento genico di nuova generazione (Next Generation Sequencing, NGS) fornisce la visione più completa di un ampio numero di geni: è in grado di analizzare oltre 300 mutazioni geniche e può individuare le alterazioni molecolari da minime quantità di tessuto. La ricerca con il test NGS può essere effettuata direttamente sul tessuto tumorale asportato oppure su un campione di sangue. In quest’ultimo caso, si parla di ‘biopsia liquida’, una tecnica che consente di studiare, nei fluidi biologici come il sangue, numerose componenti molecolari del tumore, e che può rappresentare uno strumento importante per seguire nel tempo l’evoluzione dinamica della neoplasia”.
“Un esempio paradigmatico di alternazione genica che può essere trattata con farmaci agnostici è quella del gene NTRK – sottolinea Nicola Silvestris, Membro Direttivo Nazionale AIOM e Professore Associato di Oncologia Medica IRCCS Istituto Tumori ‘Giovanni Paolo II’ di Bari – DIMO Università degli Studi di Bari – I tumori con fusione di NTRK non si limitano a specifici istotipi, ma possono interessare qualsiasi organo. L’identificazione delle neoplasie portatrici di questi riarrangiamenti genici è fondamentale per la selezione dei pazienti che possono beneficiare delle terapie mirate appartenenti alla famiglia degli inibitori della tirosin-chinasi”.
Nel 2020 in Italia sono stimati 377mila nuovi casi di tumore e 3,6 milioni di cittadini vivono dopo la diagnosi. Nella pratica clinica i test agnostici sono utilizzati soprattutto nelle neoplasie dell’apparato gastroenterico, del polmone, nei sarcomi, nei tumori urologici, ginecologici, mammari e del distretto cervico-facciale.
“L’accesso dei pazienti alle terapie agnostiche inizia con l’esecuzione di un test di profilazione genomica, prosegue con l’interpretazione dei dati, per arrivare alla scelta terapeutica – continua Rita Chiari, Membro Direttivo Nazionale AIOM e Direttore Struttura Complessa Oncologia Ospedali Riuniti Padova Sud – L’estrema complessità della gestione del modello mutazionale in oncologia richiede in maniera imprescindibile l’attivazione dei Molecular Tumor Board (MTB), gruppi interdisciplinari (formati da oncologo medico, anatomopatologo, biologo molecolare, genetista, farmacologo clinico, farmacista ospedaliero, bioinformatico, epidemiologo clinico, bioeticista e rappresentanti dei pazienti), in cui siano integrate molteplici competenze per governare i processi clinici e decisionali di appropriatezza. Oggi in Italia operano solo una decina di MTB, pertanto devono essere implementati, rispondendo a criteri comuni”.
“Inoltre – conclude il Presidente Beretta – un obiettivo cruciale è la condivisione di dati genomici uniformi mediante la creazione di una Piattaforma Nazionale Genomica, che permetterà la produzione di nuove conoscenze e l’accesso dei pazienti alle terapie innovative, consentendo al contempo la valutazione dell’efficacia e dei costi e un maggiore governo della pratica clinica. Esistono oggi varie realtà in cui sono stati attivati database con estrazione di dati strutturati e non-strutturati secondo procedure di interoperatività. La Piattaforma Nazionale condivisa non dovrà sostituire i sistemi informatici già disponibili, né creare un sistema aggiuntivo di centralizzazione dei dati, che rimarranno nella custodia dei laboratori e delle Istituzioni che li hanno generati. La Piattaforma Nazionale dovrà affiancarsi a quelle locali e creare un sistema virtuale di condivisione dei dati genomici basato sulla interoperabilità”.