Svolta nella diagnosi precoce dei tumori: microscopia innovativa per visualizzare in 3D le cellule tumorali

Uno studio internazionale, guidato da ricercatori italiani dell’Istituto di scienze applicate e sistemi intelligenti “E. Caianiello” del Consiglio nazionale delle ricerche, dell’Università degli Studi di Napoli Federico II e del CEINGE – Biotecnologie Avanzate Franco Salvatore, ha rivelato la possibilità di identificare, visualizzare e misurare in 3D il nucleo di singole cellule tumorali con l’utilizzo di tecniche avanzate di microscopia senza l’utilizzo di coloranti chimici. Lo studio, pubblicato su Nature Photonics, apre nuove strade ad applicazioni di biologia cellulare

Roma, 14 novembre 2022 – Cellule in 3D senza l’uso di coloranti chimici o anticorpi marcatori: uno studio internazionale, guidato da ricercatori italiani dell’Istituto di scienze applicate e sistemi intelligenti “E. Caianiello” (Isasi) del Consiglio nazionale delle ricerche, dell’Università degli Studi di Napoli “Federico II” e del CEINGE – Biotecnologie Avanzate Franco Salvatore, ha scoperto il sistema per fare la TAC ad ogni singola cellula distinguendo le sane dalle malate, senza alternarne la conformazione e riducendo il margine di errore nell’interpretazione umana dei dati.
Si tratta di una tomografia olografica a flusso in grado di misurare proprietà biofisiche strettamente connesse allo stato della cellula, ottenute mediante tecniche computazionali, che potrebbe determinare una svolta molto significativa nella diagnosi precoce dei tumori e nella sperimentazione di nuovi farmaci per uso terapeutico.
I risultati della ricerca, pubblicata sulla rivista scientifica di alto impatto Nature Photonics (Springer Nature Group) hanno rivelato la possibilità di identificare, visualizzare e misurare in 3D il nucleo di singole cellule tumorali con l’utilizzo di tecniche avanzate di microscopia senza l’utilizzo di coloranti chimici aprendo così strade completamente nuove per gli studi di biologia cellulare.
Questo si pensa potrà aprire la strada ad applicazioni, in futuro, nella clinica delle malattie dovute ad alterazioni molecolari. Di fatto, la tecnologia olografica laser 3D alla base dei risultati ottenuti potrà rivoluzionare la citometria a flusso, attualmente basata su imaging 2D a fluorescenza. Quest’ultima è, infatti, limitata dal processo di colorazione necessario per identificare strutture intracellulari, richiede molto tempo e potrebbe alterare le proprietà cellulari.
“L’applicazione più promettente della citometria a flusso basata sulla tomografia a contrasto di fase è la biopsia liquida, l’indagine meno invasiva attualmente praticabile, che mira alla diagnosi precoce dei tumori e alla definizione di terapie oncologiche personalizzate – spiega Achille Iolascon, professore di Genetica Medica della Federico II e Principal Investigator CEINGE assieme a Mario Capasso – La metodica di identificazione di singole cellule tumorali messa a punto in questo studio apre la possibilità di attivare nuove linee di ricerca per sviluppare tecniche in grado di monitorare ed estrarre le cellule tumorali che circolano nel sangue del paziente”.
Il team italiano che ha svolto la ricerca e che comprende fisici, ingegneri, genetisti e biotecnologi, ed è stato arricchito dalla collaborazione internazionale di ricercatori del Laboratorio di Ottica dell’Ecole Polytechnique Fédérale de Lausanne (EPFL) diretto da Demetri Psaltis.
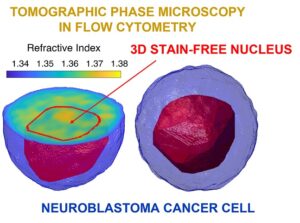
Lo studio si è focalizzato sul nucleo di cellule tumorali che, tra i vari organelli, è quello che contiene la maggior parte del materiale genetico ed è responsabile del ciclo di vita della cellula. Identificare il nucleo in cellule non marcate è una sfida enorme a cui diversi gruppi nel mondo stanno provando a dare soluzioni negli ultimi anni.
Per il Cnr-Isasi, l’attività computazione è stata svolta da Pasquale Memmolo (responsabile) e Daniele Pirone (assegnista): non potendo sfruttare lo strumento dell’intelligenza artificiale hanno sviluppato un metodo statistico ad hoc, puramente computazionale.
Lisa Miccio ha, invece, contribuito allo sviluppo del Tomografo Olografico a flusso presso i laboratori dell’Istituto: la natura 3D della tomografia a contrasto di fase a flusso ha la capacità di misurare le proprietà biofisiche strettamente connesse allo stato della cellula e – grazie all’assenza di coloranti chimici – rappresenta una vera svolta tecnologica rispetto alla citometria a flusso convenzionale.
“I risultati ottenuti aprono scenari su nuove ricerche per identificare ulteriori organelli intracellulari non marcati e per proseguire lo sviluppo verso sistemi portatili a basso costo del tipo “lab-on-chip”, prospettando l’implementazione della medicina personalizzata basata sull’analisi non invasiva di singole cellule in fluidi biologici (sangue, urine, salive, etc.)”, conclude Pietro Ferraro (Cnr-Isasi) Coordinatore nazionale del Progetto di Rilevante Interesse Nazionale dal Ministero dell’Università e della Ricerca italiano (PRIN 2017N7R2CJ denominato MORFEO-Morphological Biomarkers for early diagnosis in Oncology) che ha finanziato la ricerca.