Morte cardiaca improvvisa, scoperte cellule coinvolte nello sviluppo della malattia. Verso nuove terapie farmacologiche


Padova, 24 gennaio 2020 – Succede all’improvviso: un giovane sportivo che di colpo si accascia durante una partita o un allenamento e muore, nonostante tutti i tentativi di rianimarlo. Un evento tragico che può colpire sia semplici appassionati, sia atleti avviati a una carriera promettente.
Una delle cause più frequenti è la cardiomiopatia aritmogena, una malattia ereditaria, che interessa circa una persona ogni 5.000 e provoca due morti all’anno ogni 100mila persone sotto i 35 anni di età.

Per questa malattia, tristemente nota ai più per avere colpito atleti e calciatori famosi, non esiste, a tutt’oggi, una cura. Le misure terapeutiche attualmente disponibili sono solo palliative.
Nei portatori di specifici difetti genetici, le cellule del miocardio, prevalentemente del ventricolo destro, muoiono progressivamente e vengono sostituite da tessuto fibroso e adiposo; questo processo favorisce lo sviluppo di aritmie cardiache, quali tachicardia e fibrillazione ventricolare, che possono provocare arresto cardiaco. Nel caso di fibrillazione ventricolare, senza una pronta defibrillazione elettrica, si ha morte improvvisa in pochissimi minuti.
Nonostante siano stati scoperti numerosi geni coinvolti nella malattia, i meccanismi che portano alla morte delle cellule cardiache, alla loro sostituzione con tessuto fibro-adiposo e in generale allo sviluppo della malattia, sono ancora poco conosciuti.

In uno studio Pathogenic Potential of Hic1-Expressing Cardiac Stromal Progenitors pubblicato dalla prestigiosa rivista americana Cell Stem Cell, ricercatori dell’Università della British Columbia di Vancouver con la collaborazione di ricercatori dell’Università di Padova hanno dimostrato che il tessuto fibroso e adiposo nel miocardio affetto da cardiomiopatia aritmogena deriva da cellule specifiche chiamate FAP (progenitori fibro-adipogenici).
“Si tratta di cellule staminali multipotenti – dice la prof.ssa Paola Braghetta del Dipartimento di Medicina Molecolare dell’Università di Padova – che, se vengono attivate ad esempio in seguito ad un danno ischemico, possono rispondere differenziandosi in tessuto fibro-adiposo. Il blocco farmacologico di tale differenziamento utilizzando una molecola sperimentale ha portato ad un miglioramento della funzionalità cardiaca”.
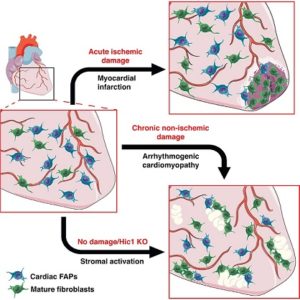
“In questo studio abbiamo utilizzato topi transgenici, generati dal nostro gruppo di ricerca – spiega la prof.ssa Alessandra Rampazzo, del Dipartimento di Biologia – i quali, una volta inserita una mutazione identificata in un paziente affetto da cardiomiopatia aritmogena, manifestano le caratteristiche patologiche riscontrate nei pazienti. Nei cuori di questi topi transgenici, queste specifiche cellule staminali vengono attivate e producono gran parte del tessuto fibroso e adiposo”.
La prof.ssa Rampazzo, che da molti anni si occupa di studiare le cause genetiche della cardiomiopatia aritmogena, riuscendo con il suo gruppo di ricerca ad identificare numerosi geni responsabili della malattia, sottolinea l’importanza della scoperta, in quanto, se da un lato apre la strada alla comprensione dei meccanismi con cui si instaura e si sviluppa la malattia, dall’altro rappresenta un importante passo avanti nell’identificare nuove terapie farmacologiche che per la prima volta porterebbero a bloccare i meccanismi molecolari e ad un arresto della progressione della malattia, invece di curare i segni clinici come le aritmie.
Visti tali importanti risultati, il gruppo della prof.ssa Rampazzo ha recentemente iniziato a studiare gli effetti di possibili molecole terapeutiche su questo nuovo tipo di cellule. Questo studio si inserisce all’interno di un programma di collaborazione scientifica e didattica che è stato recentemente sottoscritto dalle due Università coinvolte.