Leucemia linfatica cronica: nei recettori la chiave per sconfiggerla
Prof. Paolo Ghia, professore presso l’Università Vita-Salute San Raffaele e a capo del Programma di Ricerca Strategica sulla Leucemia linfatica cronica: “La scoperta è importante non solo perché offre un modello unico in grado di spiegare una grande varietà di esiti clinici, ma anche perché identifica nuovi potenziali target terapeutici”
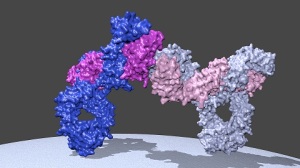
In questa figura si vedono due recettori sulla superficie di una cellula B leucemica che si legano tra loro, avviando il processo anomalo di proliferazione tumorale. Tramite cristallografia a raggi X è stato possibile visualizzare i dettagli dell’interazione, riconoscendo le regioni coinvolte e il tipo di legame. La scoperta apre la strada allo sviluppo di molecole che evitino il contatto tra i recettori e combattano così lo sviluppo della leucemia linfatica cronica
Milano, 9 giugno 2017 – La leucemia linfatica cronica è la forma di leucemia più frequente negli adulti e comporta la duplicazione incontrollata di cellule del sistema immunitario (i linfociti B), che si diffondono nel sangue, depositandosi nel midollo osseo e negli altri organi.
Un gruppo di ricercatori guidato da Paolo Ghia e da Massimo Degano, rispettivamente a capo del Programma di Ricerca Strategica sulla Leucemia linfatica cronica e dell’Unità di Biocristallografia dell’IRCCS Ospedale San Raffaele – una delle 18 strutture di eccellenza del Gruppo Ospedaliero San Donato – ha rivelato il meccanismo alla base della proliferazione delle cellule B leucemiche: i recettori sulla membrana di queste cellule, che normalmente si attivano dopo essersi legati a virus o batteri specifici, nei casi di leucemia linfatica cronica si legano a loro stessi, di fatto auto-attivandosi con intensità diversa nelle persone affette dalla malattia.
La scoperta, pubblicata su Nature Communications e resa possibile grazie al sostegno dell’Associazione Italiana per la Ricerca sul Cancro (AIRC), spiega in modo semplice la presenza di varie forme di leucemia linfatica cronica nei pazienti – dalle più aggressive alle più indolenti – e apre la strada allo studio di nuovi approcci terapeutici che colpiscano direttamente i recettori difettosi.
Le cellule B del sistema immunitario ci proteggono grazie alla loro capacità di riconoscere in modo tempestivo minacce esterne e interne all’organismo, come virus, batteri o cellule tumorali, e renderle innocue.
Per riuscire nell’impresa ogni cellula B esprime sulla sua membrana un recettore particolare, detto B Cell Receptor (BCR) o immunoglobulina. Questi recettori funzionano come delle chiavi, adatte a entrare solo in alcune serrature: la loro struttura è fatta su misura per legarsi a specifiche molecole che si trovano, ad esempio, sulla superficie di un virus o di un batterio.
Quando un recettore BCR si lega alla sua molecola corrispondente, riconoscendo quindi la presenza di una minaccia per l’organismo, attiva il processo di duplicazione della cellula B e la successiva produzione di anticorpi. Si tratta di una strategia di difesa molto efficiente, perché permette di produrre in poco tempo proprio gli anticorpi giusti per disattivare la minaccia in quel momento presente.
Nel caso della leucemia linfatica cronica alcune cellule del sistema immunitario, i linfociti B, proliferano senza controllo e sono la causa della malattia. Era già noto che i recettori di queste cellule B impazzite risultano attivati, come se stessero riconoscendo una minaccia che in realtà non è presente.
Con lo studio appena pubblicato, per la prima volta si svela il modo in cui avviene questo cortocircuito d’attivazione: i recettori sulla superficie di queste cellule si legano tra loro con intensità diverse a seconda della gravità della malattia.
La scoperta, fatta da un gruppo interdisciplinare di ricercatori – medici, biologici e biochimici – sotto la guida di Paolo Ghia e Massimo Degano, permette anche di spiegare in modo semplice la diversità delle leucemie linfatiche croniche che si osservano nei pazienti: da quelle più aggressive a quelle più indolenti e a progressione lenta.
“Il fatto che le cellule del sistema immunitario proliferino in modo particolarmente rapido o invece si duplichino con minore velocità dipende dalla stabilità del legame che si crea tra i recettori sulla loro superficie – spiega Massimo Degano, a capo dell’Unità di Biocristallografia – Se il legame è stabile le cellule B rallentano la loro duplicazione, dando origine alle forme di leucemia meno aggressive, viceversa se il legame è instabile, e continua perciò a crearsi e rompersi, le cellule sono continuamente stimolate a proliferare e danno origine alle forme di leucemia più aggressive”.
Per confermare questa ipotesi i ricercatori hanno utilizzato la cristallografia a raggi X, una tecnica che consente di visualizzare la struttura tridimensionale delle molecole, per analizzare la differenza tra il tipo di legame che si osserva nella forma di leucemia linfatica cronica più aggressiva tra quelle note (il tipo 2) e di quella al contrario più indolente (il tipo 4). Non solo, hanno fatto esprimere ciascuno di questi recettori difettosi a una cellula B dormiente, dimostrando che la loro presenza era sufficiente per attivarla.
“La scoperta è importante non solo perché offre un modello unico in grado di spiegare una grande varietà di esiti clinici, ma anche perché identifica nuovi potenziali target terapeutici – spiega Paolo Ghia, professore presso l’Università Vita-Salute San Raffaele e a capo del Programma di Ricerca Strategica sulla Leucemia linfatica cronica – I farmaci attualmente disponibili agiscono su ciò che avviene in seguito all’attivazione dei recettori, anche perché non era chiaro il meccanismo con cui questa avvenisse. Ora possiamo pensare di colpire direttamente i recettori e bloccare in modo specifico il meccanismo con cui producono questo cortocircuito”.
Oltre al sostegno fondamentale dell’Associazione Italiana per la Ricerca sul Cancro (AIRC), lo studio è stato possibile grazie al contributo di Fondazione Intesa San Paolo Onlus, Fondazione Cariplo e del Ministero della Salute Italiano.
fonte: ufficio stampa