Alzheimer, studio conferma lo squilibrio del rame ‘cattivo’ nell’organismo come fattore di rischio. Nuovi scenari terapeutici

Dott.ssa Rosanna Squitti, ricercatrice al Fatebenefratelli-Isola Tiberina di Roma e capofila dello studio: “Grazie al test del rame, effettuabile con un semplice prelievo di sangue, è possibile identificare i soggetti che hanno valori di rame non-ceruloplasminico sopra la soglia di 1,6 µmol/L per intervenire su questo fattore di rischio modificabile”
Roma, 15 luglio 2021 – L’Alzheimer, la più temuta delle demenze, colpisce oggi circa 30 milioni di persone nel mondo (di cui 600 mila solo in Italia): un processo degenerativo del cervello che compromette le principali funzioni cognitive e che rimane tra le patologie maggiormente all’attenzione di medici e ricercatori nel panorama globale.
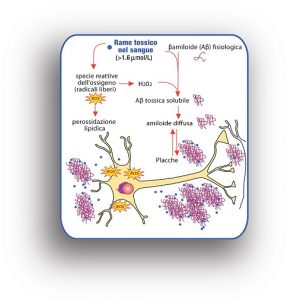
Un vasta letteratura scientifica negli anni ha supportato la tesi del rame ‘cattivo’ (non-ceruloplasminico) quale fattore di rischio per la malattia di Alzheimer: si tratta di quel rame anche detto ‘libero’ che – diversamente dal rame ‘buono’ – non si lega ad una proteina, la ceruloplasmina, attraverso la quale viene trasportato nell’organismo per contribuire allo svolgimento di importanti funzioni vitali e metaboliche. Il rame ‘fuori’ dal controllo delle proteine innesca così reazioni ossidanti che vanno a danneggiare cellule e tessuti.
Oggi, una ricerca (meta-analisi) di recente pubblicata sulla rivista internazionale Biomolecules ha esaminato 56 studi realizzati tra il 1984 e il 2020 su un totale di 6.000 soggetti, e li ha messi a confronto con un nuovo studio ‘di replica’ che ha analizzato diversi marcatori di rame e varianti del gene ATP7B associato alla sua disfunzione.

“Dalla meta-analisi condotta si evidenzia che nella malattia di Alzheimer la presenza di rame nel cervello diminuisce, mentre nel sangue aumenta. I due dati non sono in contraddizione tra loro: fanno parte di uno squilibrio sistemico tra rame ‘buono’ (legato alle proteine) che diminuisce e rame ‘cattivo’ (non legato alle proteine) che aumenta”, spiega Rosanna Squitti, ricercatrice al Fatebenefratelli-Isola Tiberina di Roma e capofila dello studio che coinvolge 6 importanti centri italiani: IRCCS Centro San Giovanni di Dio-Fatebenefratelli e Università di Brescia, Istituto Humanitas di Milano, Università di Chieti, Fondazione S. Lucia-IRCCS di Roma, Fondazione Mondino-IRCCS di Pavia, oltre al Dipartimento Ricerca e di Medicina di Laboratorio dell’Isola Tiberina.
“Questo squilibrio – continua la Squitti – è lo specchio di un altro tipo di patologia legata al rame tossico, la malattia di Wilson, assunta come paradigma per lo studio sul ruolo del metallo nell’Alzheimer. L’eccesso di rame non-ceruloplasminico aumenta di 3 volte il rischio di ammalare e lo studio ‘di replica’ (condotto su circa 170 pazienti) che abbiamo associato ai 56 studi esaminati dimostra che i portatori delle varianti-rischio del gene ATP7B sono più suscettibili ad ammalare di Alzheimer”.
Non solo. In linea di continuità con questo studio, è stato pubblicato in questi giorni sulla rivista Journal of Alzheimer Disease una sorta di ‘manifesto’ scientifico internazionale che sancisce il principio del nesso causale tra rame non-ceruloplasminico e Alzheimer e presenta le basi scientifiche per un sottotipo di malattia di Alzheimer caratterizzato appunto dalla presenza di questo squilibrio.
A firmare lo studio, con la stessa ricercatrice capofila Rosanna Squitti, un “Consorzio” internazionale di ricercatori considerati di spicco per questo settore di ricerca: Peter Faller, (Università di Strasburgo, Francia), Christelle Hureau (CNRS di Tolosa, Francia), Anthony White (QIMR Berghofer Medical Research Institute, Queensland, Australia), Alberto Granzotto (Università della California, Irvine, CA, Stati Uniti) e Kasper Kepp (Technical University della Danimarca).
Sulla base delle evidenze raccolte, in sostanza, si riassume in un costrutto teorico, dal punto di vista clinico, chimico e genetico, il legame causale tra rame e malattia di Alzheimer, ancor più sottolineato dal fatto che la proteina precursore della beta-amiloide, considerata tra i fattori killer della malattia (quella che forma le placche nel cervello con Alzheimer) è una proteina ‘a rame’, cioè ha siti di legame specifici per questo metallo.
Lo studio rafforza così il sostegno a nuovi scenari terapeutici. “Grazie al test del rame, effettuabile con un semplice prelievo del sangue – precisa la ricercatrice Squitti – è possibile identificare i soggetti che hanno valori di rame non-ceruloplasminico sopra la soglia di 1,6 µmol/L per intervenire su questo fattore di rischio modificabile, proponendo alle persone non ancora malate un cambiamento di stile di vita con una dieta a basso contenuto di rame, mentre per le persone già malate si potrebbero proporre dei trattamenti farmacologici già in commercio in grado di ridurre la presenza del rame tossico, analogamente a come si fa con la malattia di Wilson”.
“A tale proposito – conclude Squitti – abbiamo da poco iniziato un trial clinico di fase II approvato dall’AIFA e finanziato dall’Alzheimer’s Association che riguarderà persone con livelli di rame non-ceruloplasminico sopra soglia e con disturbo cognitivo lieve per verificare se il trattamento farmacologico con lo zinco possa diminuire i livelli di rame e arrestare l’evoluzione del declino cognitivo”.